全球特藥領域生物制藥公司益普生(Euronext:IPN;ADR:IPSEY)今日公布了2024年第一季度的銷售業績。
重點回顧
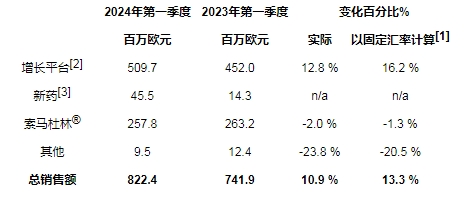
以固定匯率計算[1],總銷售額增長率為13.3%(報告為10.9%),該增長主要歸因于以下兩方面:增長平臺[2]銷售額增長16.2%[1]和新藥貢獻增加。索馬杜林銷售額僅下降1.3%[1]
Onivyde在美國獲得監管批準并上市,用于轉移性胰腺導管腺癌(mPDAC)的一線治療
確認2024年財務指引
益普生首席執行官David Loew表示:“我們在第一季度實現了出色的業績,為益普生2024年的增長奠定了堅實的基礎。在增長平臺的成功和新藥貢獻增加的支持下,我們的銷售額繼續保持強勁增長,這證明我們戰略計劃得到了成功實施。此外,研發管線也不斷傳來喜報,本季度,Onivyde在美國獲得監管批準,用于胰腺癌的一線治療。”
"今年是我們增長計劃的關鍵時期,我們將推出四款新藥或適應癥。我們的重點仍然是產品組合的表現和研發管線的擴張,以及以改善患者生活和醫療結局為中心的明確可持續增長戰略。"
2024年全年指引
益普生已確認其2024年財務指引,其中排除了任何潛在的額外后期[4]外部創新機會的影響:
以固定匯率計算,總銷售額增長超過6.0%。基于2024年3月的平均匯率水平,預計匯率將對總銷售額產生約1%的不利影響
核心營業利潤率約為總銷售額的30%,包括預期的早期和中期外部創新機會帶來的額外研發費用
總銷售額指引包括對在美國和歐盟進一步推出索馬杜林蘭瑞肽仿制藥的預期。
業務發展
2024年2月,益普生宣布美國食品藥品監督管理局(FDA)已批準Onivyde聯合奧沙利鉑、氟尿嘧啶和亞葉酸(NALIRIFOX)作為mPDAC成人患者一線治療的補充新藥申請。這是繼2015年FDA批準Onivyde聯合氟尿嘧啶和亞葉酸用于治療接受吉西他濱治療方案后出現疾病進展的mPDAC患者后,第二次批準將Onivyde方案用于治療mPDAC。在美國批準Onivyde作為mPDAC成人患者的一線治療藥物的同時,Onivyde還被授予孤兒藥獨占許可,監管獨占期持續至2031年(批準后自動啟用7年獨占期)。
2024年4月,益普生宣布就靶向ROR1腫瘤抗原的抗體偶聯藥物(ADC)STRO-003達成全球獨家許可協議。STRO-003正處于臨床前開發的最后階段。該協議賦予益普生全球獨家開發和商業化STRO-003的權利,這也是益普生不斷擴大的研發管線中的第一款ADC候選藥物。
益普生和Skyhawk Therapeutics于2024年4月宣布簽署全球獨家合作協議,共同發現和開發調節罕見神經系統疾病RNA的新型小分子藥物。該協議包括一項選擇權,根據該選擇權,益普生將獲得在全球范圍內開發成功候選藥物的獨家許可。
Onivyde訴訟
2024年3月,益普生收到關于Conjupro Biotherapeutics, Inc. (Conjupro)向美國FDA提交505(b)(2)申請的第IV段通知函,請求批準鹽酸伊立替康脂質體注射液上市,用于治療既往接受吉西他濱治療后出現進展的mPDAC患者。該信函對保護Onivyde及其用途的多項專利提出了質疑。作為回應,益普生于2024年4月向美國新澤西州地方法院對Conjupro和某些相關公司實體提起專利侵權訴訟,并將全力捍衛自身權利,因為其專利組合包括將于2027年到期的脂質體組合物的美國專利保護,以及涵蓋該制劑和批準用于治療吉西他濱治療后出現進展的mPDAC患者的其他專利(有效期至2033年,一線治療的額外保護有效期至2036年)。
說明
所有財務數據均以百萬歐元(€m)為單位。本報告的業績涵蓋2024年3月31日之前的3個月期間(2024年第一季度),而進行數據對比的對象為2023年3月31日之前的3個月期間(2023年第一季度)。
點擊【閱讀原文】,至益普生全球官網,查閱詳細報告。
注
[1]以固定匯率(CER)計算,即通過應用前一時期使用的匯率重新計算相關時期的業績,排除任何外匯影響
[2]吉適(A型肉毒毒素)、達必佳(曲普瑞林)、Cabometyx(Cabozantinib)和Onivyde(伊立替康)
[3]Bylvay(Odevixibat)、Tazverik(Tazemetostat)和Sohonos(Palovarotene)
[4]Ⅲ期臨床開發或之后
關于益普生
益普生是一家全球性的生物制藥公司,專注于在腫瘤、罕見病和神經科學三個治療領域為患者提供革新型藥物。我們的研發管線以外部創新為動力,有近百年的開發經驗以及美國、法國、英國的全球中心作為有力的支持。分布于40多個國家的全球團隊,共同與我們在世界各地的合作伙伴關系,使我們為100多個國家的患者提供藥物。益普生在巴黎(泛歐交易所:IPN)上市并通過贊助的I級美國存托憑證項目(ADR:IPSEY)在美國上市交易。有關益普生的更多信息,請訪問ipsen.com.
關于益普生中國
益普生集團于1992年進入中國,2019年在上海設立創新中心,是全球四個研發中心之一。益普生于2021年在上海成立中國區總部,并于2022年根據集團業務變動,同步剝離多元健康業務,專注于特藥領域,針對三大疾病領域(腫瘤、罕見病、神經科學)攜手上海創新中心持續推出創新治療方案以滿足中國患者亟待解決的治療需求。
益普生-有關前瞻性聲明的警示說明
本文所含前瞻性聲明、目的和目標基于集團的管理戰略、當前觀點和假設。此類聲明涉及已知和未知的風險和不確定性,可能導致實際結果、業績或事件與本文所預期的大不相同。上述所有風險均可能影響集團在未來實現其財務目標的能力,財務目標是基于現今可用信息在合理的宏觀經濟條件下設定的。"相信"、"期望"和"期待"等詞語和類似表述的使用是為了明確前瞻性聲明,包括集團對未來事件的期望,此類事件包括監管文件和決定。此外,本文所述目標的制定未考慮外部增長假設和潛在未來收購,而這兩者可能會使指標發生變化。目的的依據是集團認為合理的數據和假設。目標取決于將來可能發生的條件或事實,而不僅取決于歷史數據。考慮到某些風險和不確定性的發生,實際結果可能與這些指標有很大出入,明顯表現為在早期研發階段或臨床試驗中有前景的產品可能最終永遠不會投放市場或達到其商業目標,尤其是由于注冊或競爭原因。集團必須面對或可能面對來自仿制藥的競爭,這可能會轉化為市場份額的損失。此外,研發過程涉及多個階段,每個階段都涉及重大風險,即集團可能無法實現其目的并被迫放棄就自身已投入大量資金的產品所做的努力。因此,集團不能確定在臨床前試驗中獲得的有利結果是否會在隨后的臨床試驗中得到確認,也不能確定臨床試驗的結果是否足以證明相關產品的安全性和有效性。不能保證產品將獲得必要的注冊批準或該產品將被證明在商業上是成功的。如果基本假設證明不準確或確實出現風險或不確定性,則實際結果可能與前瞻性聲明中的結果有很大不同。其他風險和不確定性包括但不限于一般行業條件和競爭;一般經濟因素,包括利率和貨幣匯率波動;制藥行業法規和醫療保健立法的影響;全球醫療成本抑制趨勢;競爭對手獲得技術進步、新產品和專利;新產品研發中固有的挑戰,包括獲得監管部門的批準;集團準確預測未來市場狀況的能力;生產困難或延誤;國際經濟的金融不穩定和主權風險;對集團專利的有效性和創新產品的其他保護的依賴;以及可能面臨的訴訟,包括專利訴訟和/或監管訴訟。此外,集團依賴第三方來研發和銷售某些產品,這些產品可能會產生大額特許權使用費用;這些合作伙伴的行為可能會對集團的活動和財務結果造成損害。集團不能確定其合作伙伴將履行各自的義務。集團可能無法從這些協議中獲得任何利益。集團任何合作伙伴違約均會產生低于預期的收益。此類情況可能會對集團的業務、財務狀況或業績產生負面影響。集團明確聲明,除非適用法律有所要求,否則其不承擔更新或修訂本新聞稿中所包含的任何前瞻性聲明、目標或假設的任何義務,以反映此類聲明所依據的事件、條件、假設或情況的任何變化,也不會就此作出任何承諾。集團的業務受制于其在法國金融市場監管機構備案的注冊文件中概述的風險因素。該文件中所列風險和不確定性并非詳盡無遺,建議讀者參閱集團網站(www.ipsen.com)上集團的最新通用注冊文件。